全球首创!i-NYS植入式眼部肌肉神经刺激器获批上市,眼球震颤治疗迎来“中国方案”
 发布时间:2026-03-18
发布时间:2026-03-18
 信息来源:中关村生命科学园公司微信公众号
字体:
大
中
小
信息来源:中关村生命科学园公司微信公众号
字体:
大
中
小
 打印
打印
 发布时间:2026-03-18
发布时间:2026-03-18
 信息来源:中关村生命科学园公司微信公众号
信息来源:中关村生命科学园公司微信公众号
3月13日,全球首创用于先天性眼球震颤治疗的三类有源植入式医疗器械“i-NYS植入式眼部肌肉神经刺激器”正式获国家药监局(NMPA)批准上市(注册证号:国械注准20263120535)。
该产品已于2024年1月进入国家药监局创新医疗器械“绿色通道”,并于2025年6月获美国FDA的HUD认定。中美双重认证的全球首创产品在中国率先获批,彰显了中国创新实力与审评效率。
i-NYS的上市,让先天性眼球震颤这一“不治之症”的临床治疗,正式迈入全新阶段。
全球首创,突破先天性眼球震颤治疗困境
先天性眼球震颤(Congenital Nystagmus,CN)是一种先天遗传性眼疾,发生于出生时或出生后6个月内,通常伴随终身。特征为眼球不自主的节律性跳动或摆动。该病症常导致视力下降、双眼视功能障碍及异常头位,严重影响患者生活质量。据统计,我国约有130万患者,全球患者约700万。由于长期以来缺乏有效的治疗手段,该病一直被视为眼科“不治之症”。

超目科技基于超目科技创始人、北京大学人民医院眼科王乐今教授的核心技术成果研发出全球首创的“i-NYS植入式眼部肌肉神经刺激器”,首次将神经电刺激技术应用于先天性眼球震颤治疗领域,通过特定参数的电流刺激眼肌及相关神经,对患者实施精准的个体化电刺激干预,可实现眼球震颤症状和视觉质量改善的治疗效果。i-NYS的上市,将为先天性眼球震颤患者提供全新的治疗选择。
初心为引,岁月为证:一项技术二十年的稳健长跑
“您能让我的眼睛也休息一下吗?”
二十多年前,一位患有先天性眼球震颤的8岁小女孩稚嫩的询问,深深触动了王乐今教授,成为他日夜思索、灵感初现的起点。
从临床概念的初步成形到治疗原理的反复验证,再到样机研制及全国多中心临床试验的扎实展开,历经二十余年潜心的探索与攻关,最终成功将“i-NYS”系统从实验室推向了临床应用。
期间,超目科技联合创始人、北京工业大学王文思教授带领研发与生产团队,围绕植入式神经刺激系统的核心技术展开深入研究,重点攻克刺激电路架构设计、植入式电子系统实现及程控平台开发等关键技术,团队相继完成了样机研制、专用芯片设计、动物实验,并系统评估了生物相容性与手术植入可行性等多方面技术问题,为产品的临床转化奠定了坚实基础。
在此基础上,团队持续推进产品原型优化、系统集成、批量化可靠生产及全流程质量检测等工作,逐步建立起覆盖研发、工程转化到规模化生产的技术闭环,有力保障了“i-NYS”系统的高质量转化与落地应用。
2024年1月,i-NYS进入国家药监局创新医疗器械特别审查“绿色通道”,2025年6月,获得美国FDA的HUD认定;2026年3月正式获得国家药品监督管理局(NMPA)批准上市。
二十载磨砺,i-NYS研发之路
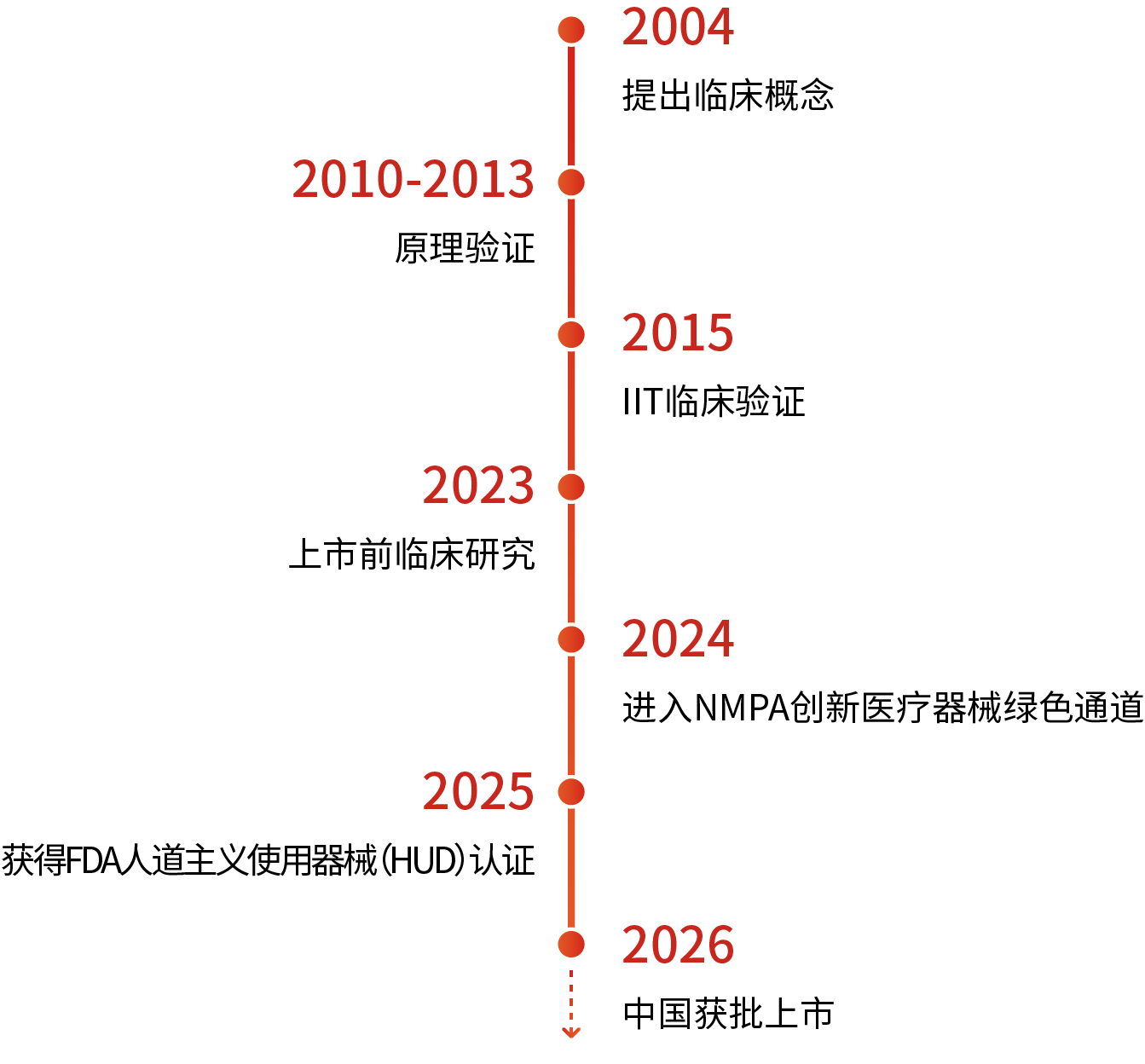
临床试验效果显著:有效性与安全性成功验证
“i-NYS植入式眼部肌肉神经刺激器”临床试验在首都医科大学附属北京朝阳医院、北京同仁医院、北京儿童医院完成。共入组71例先天性眼球震颤受试者,包括26名未成年人(8≤年龄<18 岁),45名成年人(年龄≥18 岁)。该71例受试者均接受i-NYS植入术,术后一个月开机并给予最佳治疗参数,进行个性化治疗。术后6个月随访显示,受试者黄斑中心凹注视时间(FP)提升587%,眼球震颤视功能评分(NAFX)增加65.4%,震颤幅度(NA)和震颤频率(NF)分别下降84.1%和79.4%。受试者评价指标存在统计学差异,相比于治疗前,获得显著改善。同时,71例受试者均未发生与手术相关的不良事件。
该临床试验结果表明,i-NYS可有效提升先天性眼球震颤患者黄斑中心凹注视时间,显著改善震颤症状,提高视觉质量。
中国引领:创新医疗科技惠及全球
全球首款先天性眼球震颤治疗医疗器械首发获批于中国,也充分体现了我国在高端医疗器械领域的创新实力与审评审批效率,也是“健康中国”战略下,解决临床急需、普惠民生的重要成果。该突破不仅为中国患者带来了率先治疗的机会,也为全球先天性眼球震颤治疗树立了全新的标准和方向,未来有望惠及世界各地的患者。
相关人物














