北京脑所Koziol团队发现AD关键“清障开关”:抑制它或可逆转认知缺陷
 发布时间:2026-03-24
发布时间:2026-03-24
 信息来源:中关村生命科学园公司微信公众号
字体:
大
中
小
信息来源:中关村生命科学园公司微信公众号
字体:
大
中
小
 打印
打印
 发布时间:2026-03-24
发布时间:2026-03-24
 信息来源:中关村生命科学园公司微信公众号
信息来源:中关村生命科学园公司微信公众号
3月11日,北京脑科学与类脑研究所Magdalena J. Koziol团队在Advanced Science期刊在线发表了题为“ALKBH3 m1A Demethylase Deficiency Reduces Alzheimer’s Amyloid-β Pathology”的研究论文,首次揭示ALKBH3介导的m1A去甲基化酶功能缺陷能够显著减轻AD相关的淀粉样蛋白病理。

该研究显示,在AD患者及模型小鼠脑中,去甲基化酶ALKBH3的表达水平异常升高,进而特异性“擦除”线粒体自噬关键分子PINK1 mRNA上的m1A修饰位点。这一表观修饰的丢失直接阻碍了线粒体自噬过程,使受损线粒体在神经元内部大量堆积,继而引发神经结构损伤及认知能力下降。值得注意的是,降低ALKBH3的表达能够有效减少Aβ斑块沉积并逆转认知损伤。这一发现不仅揭示了RNA甲基化在神经退行性疾病中的调控新机制,也为AD的药物开发提供了具有潜力的新靶点。
关键发现一:m1A修饰减少是AD脑中的早期事件,ALKBH3是“罪魁祸首”
研究发现,在AD小鼠和患者的核心记忆脑区——海马中,m1A修饰水平显著降低,而这一变化源于负责移除该修饰的酶ALKBH3的异常升高。无论是通过基因敲除手段抑制Alkbh3,还是使用其小分子抑制剂HUHS015干预,均能有效恢复m1A水平并显著减少病理性Aβ斑块。相反,若在脑中过表达Alkbh3,则会加剧病理进程。这表明,靶向抑制ALKBH3可能成为干预AD的全新策略。
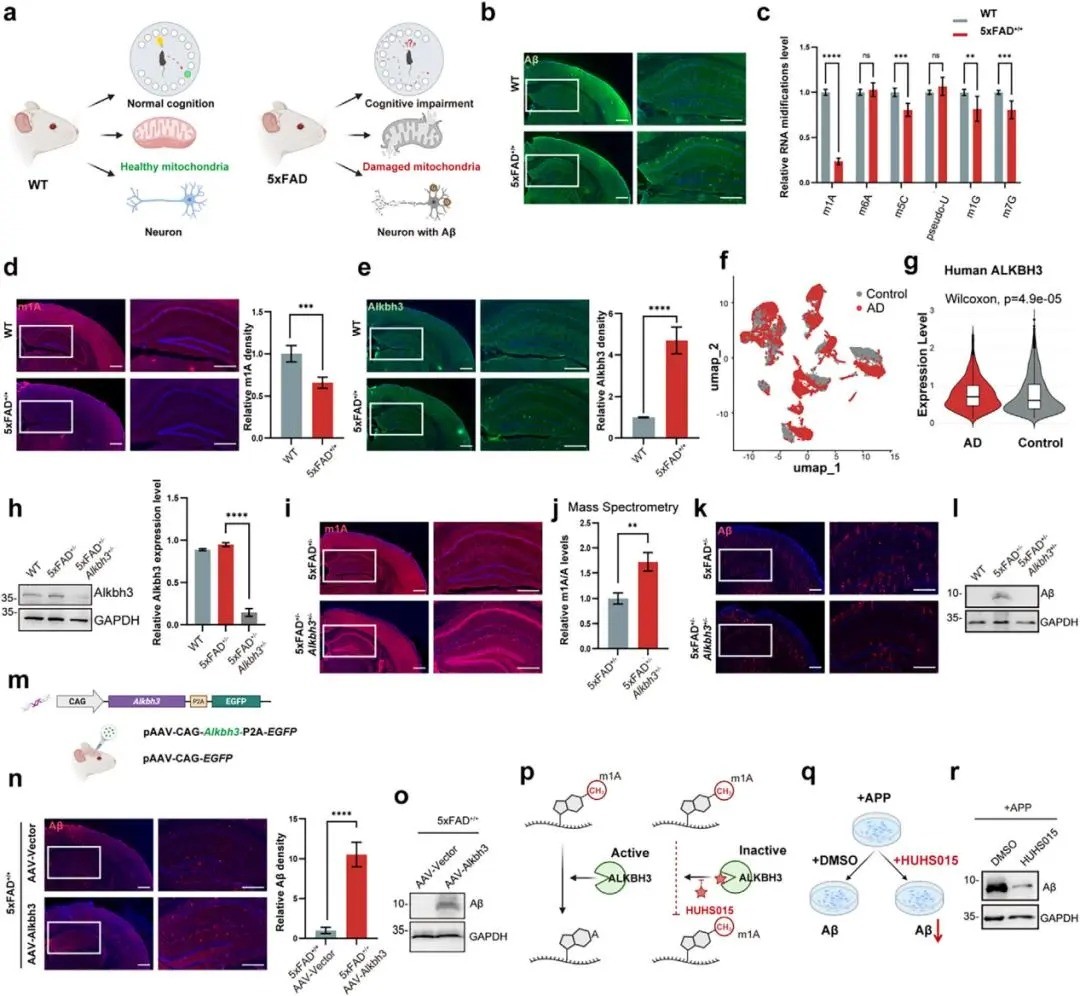
图一 Alkbh3调节5xFAD小鼠海马中的m1A和Aβ
关键发现二:抑制ALKBH3可逆转空间记忆障碍并修复神经元钙稳态
行为学实验(巴恩斯迷宫)进一步证实,降低ALKBH3水平能够完全逆转AD模型小鼠的空间学习记忆缺陷。机制解析表明,ALKBH3在神经元中扮演着“钙信号门控”的角色:其异常升高会使钙信号传导受阻,而抑制该分子则能恢复海马区钙活动,并促进树突分支及突触结构的重建。也就是说,靶向ALKBH3不仅修复了神经元的信息传导通路(钙动力学),还强化了大脑的“结构硬件”(突触可塑性),从而实现认知功能的精准修复。
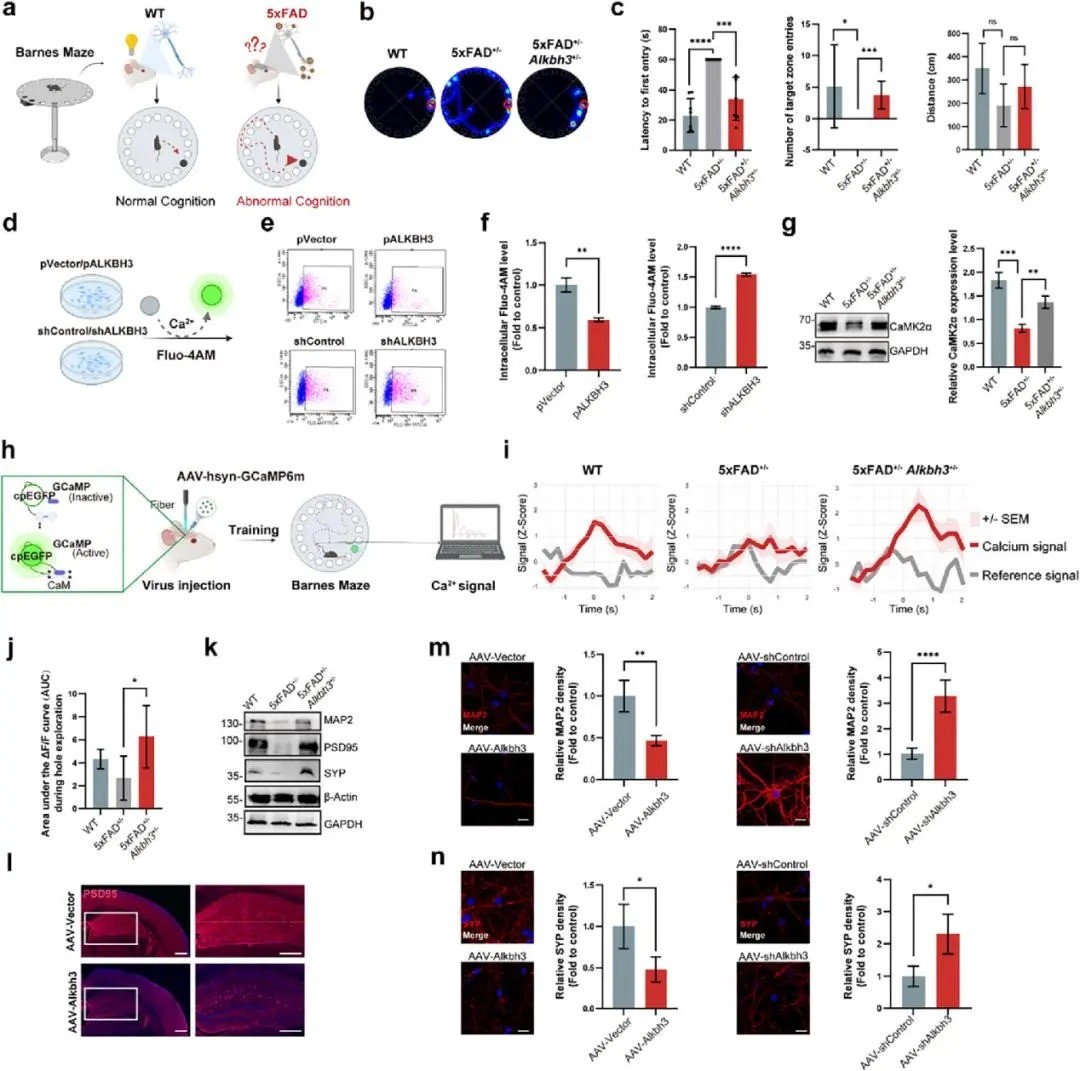
图二 ALKBH3缺失挽救了5xFAD小鼠的空间记忆障碍和钙稳态失调
关键发现三:ALKBH3通过m1A修饰调控PINK1 mRNA稳定性,影响线粒体自噬
在揭示了下游病理变化之后,研究进一步溯源上游机制:ALKBH3如何调控线粒体自噬?实验表明,ALKBH3能够直接结合PINK1 mRNA并去除其m1A修饰,导致该转录本稳定性显著下降——相当于给PINK1下达了“快速降解”的指令,使其半衰期大幅缩短,最终导致PINK1蛋白匮乏。由于PINK1是启动线粒体自噬的核心因子,其缺失直接导致受损线粒体清除障碍、毒性累积。人类样本数据也证实了ALKBH3与PINK1表达之间的显著负相关。这一发现将RNA表观调控与线粒体功能障碍直接联系起来,提示通过保护PINK1 mRNA的m1A修饰或抑制ALKBH3活性,可能重启大脑的“清洁系统”,对抗神经退行性进程。
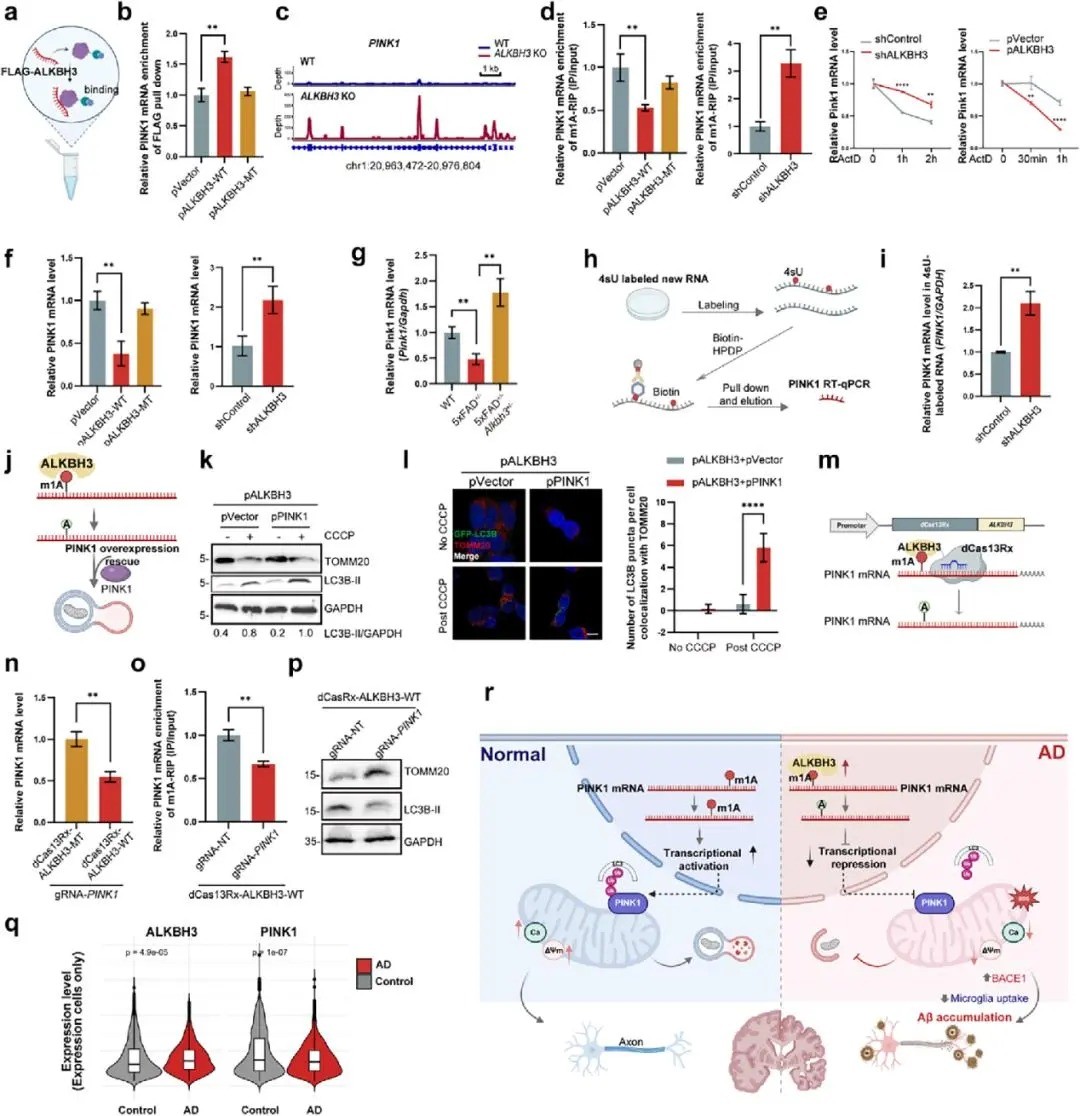
图三 ALKBH3通过依赖m1A的mRNA修饰调控PINK1
总结与展望
综上所述,ALKBH3-m1A-PINK1调控轴不仅是线粒体功能障碍的早期生物标志物,更是一个极具前景的药物干预靶点。此外,初步数据显示ALKBH3可能还参与Tau蛋白磷酸化调控,暗示其在更广泛的AD病理级联反应中扮演重要角色。该研究为理解阿尔茨海默病的表观转录组调控机制提供了新视角,也为靶向ALKBH3的干预策略奠定了坚实的理论基础。
相关人物














